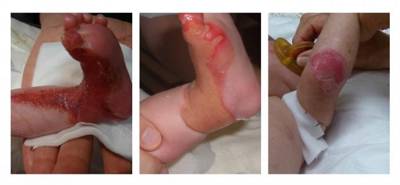
Zo voelt het leven als je EB hebt
Mendelioomanalyse
- Een nieuwe aanpak
- Wat is "massief parallelle sequenering"?
- Waarom een exoom of een mendelioom?
- Wat kan men verwachten van zo’n analyse?
- Wat heeft men nodig voor dit onderzoek?
- In welke mate is deze technologie vandaag beschikbaar voor genetisch onderzoek van een patiënt?
- Waarom is mendelioomanalyse belangrijk voor epidermolysis bullosa?
- Auteurs & info
Een exoom, een mendelioom: een nieuwe sterke aanpak voor de genetische diagnostiek van erfelijke huidaandoeningen
Een nieuwe aanpak
Het menselijk genoom bevat ongeveer 21.000 genen. Daarvan zijn er minstens een 200-tal betrokken bij erfelijke huidaandoeningen (of genodermatosen) waaronder de verschillende vormen van epidermolysis bullosa, van ichthyosis en meer zeldzame huidaandoeningen.
Nieuwe technieken, gebaseerd op wat men noemt de ‘massieve parallelle sequencing’, laten toe om al deze genen tegelijk na te kijken. De techniek is dus belangrijk om klinische aandoeningen met een zeer uiteenlopende genetische achtergrond snel te bestuderen, en op die manier sneller tot een genetische diagnose te komen.
Een van de technieken is een analyse van een exoom. Exoom is een technische term voor de som van alle genen: de 21.000 genen van ons genoom kunnen ‘in parallel’ nagekeken worden. Vergelijk je een gen met een recept (voor het aanmaken van één van de duizenden eiwitten in ons lichaam), dan kan je een exoom het best vergelijken met het volledige menselijke kookboek.
Omdat een exoom ook genen bevat waarvan de functie niet is gekend, of die alleszins (nog) niet gekoppeld werden aan een aandoening, is het enigszins overdadig om het volledige exoom na te kijken. Bovendien is een exoomanalyse duur en tijdrovend. Daarom werden door verschillende genetische centra ‘mendeliomen’ of ‘klinische exomen’ ontwikkeld: ze bevatten alle genen die tot op vandaag met erfelijke ziekten zijn geassocieerd. De inhoud van zo’n mendelioom ligt dus rond de 6000 genen, wat een besparing oplevert: de kost van de sequenering ligt lager wanneer slechts een derde van het totale aantal genen bij de mens wordt nagekeken.
Het werk wordt verder vereenvoudigd door het definiëren van ‘genpanels’. Vanuit een diagnostisch oogpunt heeft het geen zin om voor erfelijke huidafwijkingen genen na te kijken die op geen enkele manier een rol spelen bij deze aandoeningen. Het diagnostisch laboratorium heeft daarom, in overleg met de dermatologen en klinisch genetici, een lijst opgesteld van de (gekende) genen die een rol spelen bij de erfelijke huidaandoeningen.
Wanneer een patiënt op zoek is naar een genetische diagnose worden dus enkel de overeenkomstige genen nagekeken. Dit heeft twee voordelen en één nadeel. Het onderzoek is gericht op de gekende genen en verloopt sneller, en is daardoor ook goedkoper. Maar omdat het om gekende genen gaat, is er geen verdere research mogelijk indien er geen afwijking gevonden wordt in één van de gekende genen. Daarvoor moet dan weer een ander exoom worden nagekeken.
Wat is "massief parallelle sequenering"?
In onze cellen zit de genetische informatie opgeslagen in de kern. Elke cel bevat het volledige genoom van het individu. Deze genetische informatie bestaat uit ongeveer 3 miljard ‘letters’ onder de vorm van A, C, G en T (dit zijn de 4 letters die gegeven worden aan de 4 scheikundige bouwblokken van het DNA). Maar slechts 1 tot 1.5 percent van deze 3 miljard letters zitten in genen. De rest wordt nogal meewarig ‘junk DNA’ genoemd, hoewel iedereen beseft dat de cel en de natuur wellicht geen 3 miljard lettertekens zomaar voor niks bij elke celdeling laat kopiëren.
De 1 tot 1.5 percent ‘coderend DNA’ komt overeen met ongeveer 21.000 genen. Het kan verrassend klinken, maar 21.000 genen of ‘recepten’ volstaan dus om een mens te maken. De genen coderen voor eiwitten. De eiwitten zijn de bouwstenen van het menselijk lichaam.
Sommige van deze eiwitten zijn zeer specifiek voor bepaalde cellen en weefsels. Voorbeelden zijn de keratines en de collagenen en andere bindweefselmoleculen, en ook de enzymen die een rol spelen in de aanmaak en het afwerken van deze eiwitten, die uitsluitend aanwezig zijn in huid, haar en nagels.
Er zijn daarnaast ook genen die coderen voor eiwitten die in verschillende weefsels en dus niet enkel in de huid een rol spelen. Zo zijn er duizenden functies in de cel en in het lichaam die afhangen van eiwitten. Eiwitten komen tussen in het onderhoud van alle cellen, in de energiebevoorrading, in het verwerken van voedingsmiddelen en vetten. Er zijn specifieke leverenzymen, stollingsenzymen, insuline voor de afbraak van suiker, enzoverder.
Het lezen van de 3 miljard letters – of zo’n 3 tot 5 miljoen letters indien we ons beperken tot de genen – is geen sinecure. De eerste technieken voor DNA sequenering lieten toe om het genoom en de genen te lezen à rato van 250 tot 500 letters in wat men noemt een ‘run’. Deze techniek is dus nuttig om bij een patiënt één gen na te kijken, en dan desgevallend nog één, maar snel wordt het te omslachtig en te duur. Laat staan dat men met deze techniek het volledige genoom van een individu zou kunnen nalezen. Eén keer is dat gelukt, met het ‘Humaan genoom project’, een internationale inspanning die 15 jaar en een miljard dollar heeft gekost.
In de voorbije jaren zijn technieken ontwikkeld die het sequeneren van DNA met een factor 10.000 hebben versneld: men kan nu in enkele dagen enkele miljoen tot een miljard letters lezen. Dit maakt het dus mogelijk om voor individuele patiënten het volledige genoom in kaart te brengen.
Concreet wordt er ‘parallel’ gesequeneerd: men heeft niet zozeer de scheikundige techniek voor het aflezen van een DNA-sequentie veranderd – de techniek bestaat intussen meer dan 30 jaar – maar men heeft er, aan de hand van miniaturisatie en het gebruik van nanotechnologie, voor gezorgd dan de scheikundige reacties honderdduizenden tot miljoenen keren tegelijk worden toegepast, op telkens een ander stukje DNA. Wanneer dan al die letters – vergelijk het met het lezen van één zin – samen gepuzzeld worden, krijgt men dus de volledige sequentie van een gen, en eventueel van een heel genoom. Om de vergelijking door te trekken: men kan met deze technologie meteen de volledige encyclopedie – of het volledige kookboek lezen, in enkele dagen tijd.
De uitdaging, dat is duidelijk, is het interpreteren van al deze gegevens, en de zoektocht naar de (typ)foutjes in het gen of genoom. Dat laatste is het werk van de experten in het genetisch laboratorium, die hierbij gebruik maken van krachtige software die zoektocht en de interpretatie versnelt. Het resultaat – vanuit een klinisch oogpunt – is een verslag van de analyse met daarin, indien de uitslag positief is, de mutatie(s) die in één of meerdere genen werd(en) gevonden bij de patiënt.
Het is duidelijk dat deze technieken voor een revolutie hebben gezorgd voor wetenschappelijk onderzoek naar erfelijke ziekten. En ze worden in toenemende mate gebruikt in de klinische diagnostiek. Een analyse van een genoom van een patiënt ligt dus binnen handbereik. Dit betekent: vandaag is het nog te duur, maar over een paar jaar wordt het vanzelfsprekend om voor elke patiënt met een onverklaard ziektebeeld een volledige genetische analyse aan te bieden.
Waarom een exoom of een mendelioom?
Een volledige genoomanalyse is vandaag te duur en te omslachtig.
Het is op dit moment gemakkelijker om alle genen – of tenminste die genen waarvan een link met een genetische aandoening is gekend – tegelijk en dus in parallel te sequeneren.
Om de efficiëntie van het onderzoek nog te verhogen wordt met gerichte softwaretools een genpanel gedistilleerd met enkel de genen die een rol spelen bij erfelijke huidaandoeningen.
Wat kan men verwachten van zo’n analyse?
Er zijn vier verschillende mogelijkheden:
- Men vindt een genetische afwijking waarvan, op basis van de wetenschappelijke literatuur en de verworven kennis, zeker is dat ze de oorzaak is van de erfelijke huidafwijking. Op dat ogenblik is de diagnose bij een patiënt genetisch bevestigd, en kan, indien nodig of gewenst, gericht familieonderzoek worden aangeboden.
- Men vindt een genetische afwijking waarvan men niet zeker is dat ze de aandoening veroorzaakt. In dat geval is verder onderzoek nodig, bijvoorbeeld bij de ouders, om na te gaan of zij al of niet dezelfde genetische afwijking vertonen zonder dat ze de ziekte vertonen. Wanneer verschillende familieleden dezelfde aandoening vertonen zal men nagaan of zij allen dezelfde genetische afwijking vertonen. Op die manier verzamelt men, met medewerking van de familie, nuttige informatie voor de interpretatie van het genetisch resultaat.
- Men vindt geen genetische afwijking. In dat geval is de diagnose niet genetisch bevestigd. Dat sluit echter een genetische oorzaak van de huidafwijking niet uit, ze laat zich enkel moeilijk opsporen met de huidige kennis van de genetische mechanismen die aan de basis kunnen liggen van genetische aandoeningen. Bij sommige patiënten zal men dan verder wetenschappelijk onderzoek uitvoeren om nieuwe genetische afwijkingen op te sporen.
- Er worden één of meer genetische afwijkingen gevonden die de aandoening niet kunnen verklaren maar die mogelijk klinisch belang hebben. In dat geval hangt het af van de keuze van de patiënt of de ouders of ze de resultaten willen kennen, die dan kunnen meegedeeld worden tijdens een genetische raadpleging. In zo’n geval blijft de bevestiging van de klinische diagnose van de patiënt ook genetisch onverklaard.
Wat heeft men nodig voor dit onderzoek?
Het onderzoek gebeurt op een bloedstaal, uitzonderlijk op een huidbiopt, eventueel op DNA geïsoleerd uit een wangwisser. Het resultaat kan verschillende weken op zich laten wachten, afhankelijk van de complexiteit van het onderzoek.
In Leuven werd door de dermatologen en klinisch genetici een speciale, gemeenschappelijke consultatie opgericht voor genodermatosen. Een verwijzing naar zo’n raadpleging kan zorgen voor een snellere diagnose, omdat door de gedeelde expertise van de artsen vaak gericht vragen voor specifieke diagnoses kunnen gesteld worden aan het laboratorium.
In welke mate is deze technologie vandaag beschikbaar voor genetisch onderzoek van een patiënt?
De verschillende genetische centra in België hebben de nieuwe technologie voor massief parallelle sequenering ingevoerd voor de diagnostiek van erfelijke aandoeningen.
Nationaal wordt het werk verdeeld, waarbij het centrum in Leuven zich onder andere op genodermatosen heeft gericht.
Voorheen werd het onderzoek per gen aangevraagd, en vaak was de overeenkomstige test enkel in het buitenland beschikbaar. Daardoor kon de kost voor de ziekteverzekering hoog oplopen. Vaak bleef, gezien de beperkte gevoeligheid van de individuele test, het resultaat negatief.
Door meteen alle gekende genen na te kijken worden meer gevallen in korte tijd, en aan een lagere totale kost, opgelost. De centra streven er ook naar de analyses in de toekomst nog sneller af te werken.
Waarom is mendelioomanalyse belangrijk voor epidermolysis bullosa?
Hoewel een gemeenschappelijk kenmerk van alle epidermolysis bullosa (EB) patiënten is dat ze bij het minste trauma blaren ontwikkelen, kan EB zeer uiteenlopende vormen aannemen naargelang het subtype en is de genetische achtergrond zeer divers. Er zijn immers vele eiwitten betrokken bij het aan elkaar vasthouden van de verschillende huidlagen. Op dit moment zijn er al meer dan 20 genen bekend die één of andere vorm van EB kunnen geven.
Een bijkomend probleem om een makkelijke genetische diagnose te maken, is dat vele subtypen van EB op elkaar lijken, zeker gedurende de eerste levensjaren. Op die leeftijd zijn bijvoorbeeld vergroeiingen van de vingers, die zo typisch zijn voor de dystrofische vormen, nog niet opgetreden. Daarenboven is het zo dat zelfs een subtype waarbij de splitsing op hetzelfde niveau van de huid plaatsgrijpt of nog sterker, waarbij hetzelfde eiwit betrokken is, toch nog door een defect in verschillende genen kan veroorzaakt zijn. Als je maar één gen zou onderzoeken zou het dus echt wel een gok zijn.
Het kan helpen om op een biopsie via antigen mapping te kijken of bepaalde eiwitten in normale hoeveelheden aanwezig zijn, maar hiervoor is enige ervaring vereist en bovendien is deze techniek niet kostenlonend als er maar af en toe een diagnose gesteld moet worden.
Met de mendelioomanalyse is het nu mogelijk om zonder al te veel klinische of histologische (op een biopsie) informatie te hebben, toch het gendefect op te sporen. Dit lukt uiteraard enkel indien het overeenkomstige gen al aan EB gekoppeld is. Immers inherent aan een mendelioomanalyse is dat enkel die genen nagekeken worden, waarvan bekend is dat ze een genetische aandoening veroorzaken. En af en toe is het inderdaad zo dat het defect zich toch in een gen dat tot nu toe niet met EB geassocieerd is, of in een stukje van een gekend gen dat niet goed vertegenwoordigd is in het mendelioom, bevindt.
Meestal geven we wel een hint aan de moleculair geneticus welk subtype bij een bepaalde patiënt het meest waarschijnlijk is, dus welke genen ze best eerst nakijken. Wanneer er echter geen mutatie gevonden wordt, kan het rijtje van genen welke we in het panel voor blaarziekten ondergebracht hebben, verder afgelopen worden. Hiervoor is geen bijkomende sequenering nodig. Het is echter wel een opgave om het genpanel zo snel mogelijk te updaten, wanneer een nieuw gendefect voor EB ontdekt wordt.
Op deze manier hebben we de laatste drie jaar van de 15 families die met het mendelioom en blaarpanel werden onderzocht, bij 12 families het verantwoordelijke gendefect gevonden. Bij de verwanten wordt nadien enkel deze specifieke mutatie bekeken om dragerschap te onderzoeken.
De mendelioomanalyse laat ons dus toe om het histologisch onderzoek en antigen mapping op een huidbiopsie over te slaan. Dit leidt tegelijk tot besparingen, dus ook onze zorgverzekering vaart er wel bij! Enkel bij pasgeboren baby’s worden deze analyses nog systematisch gedaan, omdat we via een biopsie sneller met grote waarschijnlijkheid kunnen voorspellen dat het al dan niet om een ernstige junctionele of dystrofische vorm van EB gaat. Dit is belangrijke informatie die de manier van verzorgen en zeker ook de uitleg aan de ouders beïnvloedt.
Deze informatie over het gendefect is onmisbaar voor ouderparen die pre-implantatie genetische diagnostiek (PGD) overwegen en in de toekomst voor eventuele behandelingen met proteïne-, cel- of gentherapie.
Auteurs & info
Dank aan Dr. Marianne Morren en Prof. Gert Matthijs voor de redactie van dit hoofdstuk.
Het gespecialiseerde team in Leuven bestaat uit Dr. Marianne Morren, Prof. Eric Legius, Dr. Ellen Denayer, Prof. Gunnar Naulaers (clinici) en dr. ir. Anniek Corveleyn (moleculair geneticus).
Meer lezen?
- Voor wie meer wil weten over genen en genomen, en over het klinisch belang en de maatschappelijke gevolgen van een genoomanalyse raden we het boek ‘Iedereen GENiaal’ van Pascal Borry en Gert Matthijs aan (uitgegeven bij Ballon Media en beschikbaar in de boekhandel).
- VIB brochure "Erfelijkheid aan genen zijde".